یک جهان یک مبارزه
-همکاری بین المللی برای ایجاد یک جامعه جهانی از سرنوشت مشترک که به چالش همه گیر Covid-19 پاسخ می دهد
رمان کروناویروس که در سراسر جهان جارو شده است ، منجر به یک بحران همه گیر جهانی Covid-19 شده است. رمان Coronavirus هیچ مرز ندارد ، هیچ کشوری از این نبرد علیه Covid-19 نجات نخواهد یافت. در پاسخ به این بیماری همه گیر Covid-19 در سراسر جهان ، Liming Products Corp برای حمایت از بهزیستی جوامع جهانی ما کمک می کند.
دنیای ما در حال حاضر با تأثیر بی سابقه ای از همه گیر رمان Coronavirus 2019 (Covid-19) همه گیر است. تا به امروز ، هیچ داروی کارآمد برای درمان این بیماری در دسترس نیست. با این حال ، بسیاری از آزمایشات تشخیصی برای تشخیص COVID-19 انجام شده است. این آزمایشات بر اساس روشهای مولکولی یا سرولوژیکی برای تشخیص اسید نوکلئیک خاص کرونوویروس رمان یا نشانگرهای آنتی بادی انجام می شود. از آنجا که Covid-19 به وضعیت همه گیر رسیده است ، تشخیص زودرس عفونت کروناویروس رمان در ارزیابی شیوع ویروس و حاوی آن بسیار مهم است ، اما هنوز یک آزمایش عالی برای استفاده جهانی وجود ندارد. ما باید بدانیم که از چه آزمایشاتی می توان برای غربالگری ، تشخیص و نظارت بر عفونت COVID-19 استفاده کرد و محدودیت های آنها چیست. بسیار مهم است که چگونه می توان از این ابزارهای علمی بهتر استفاده کرد و به شناسایی و کنترل ظهور این بیماری به سرعت در حال گسترش و جدی کمک کرد.
هدف از تشخیص کرونوویروس رمان ، تعیین اینکه آیا فردی که دارای عفونت COVID-19 است یا یک ناقل بدون علامت که ممکن است ویروس را به صورت سکوت پخش کند ، برای تهیه اطلاعات اساسی برای راهنمایی تصمیم گیری برای درمان بالینی ارائه می دهد. مطالعات قبلی نشان داده اند که 70 ٪ از تصمیمات بالینی به نتایج آزمایش بستگی دارد. هنگامی که از روش های مختلف تشخیص استفاده می شود ، الزامات کیت های معرف تشخیص نیز متفاوت است.
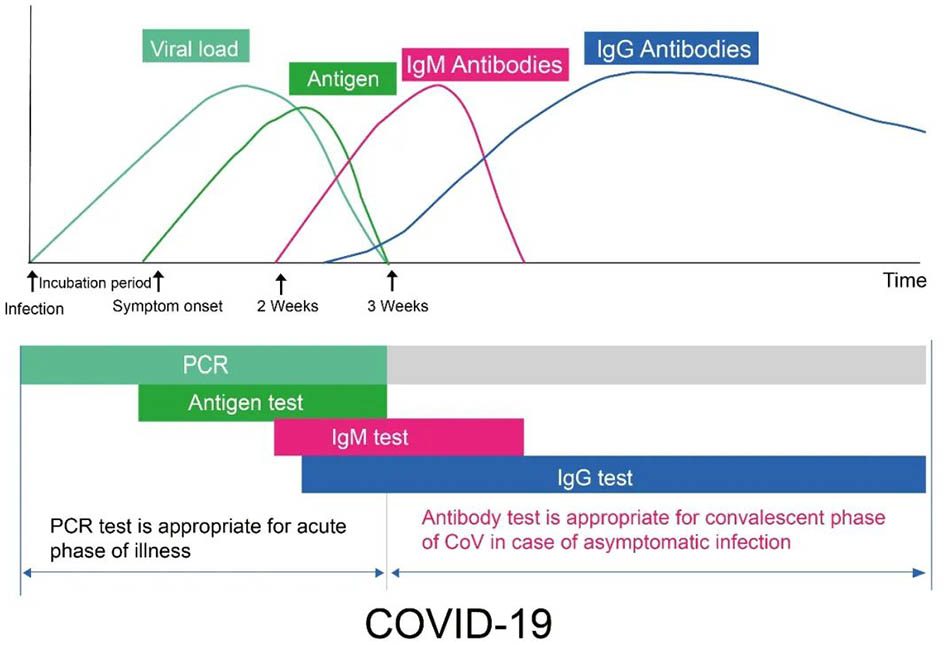
شکل 1
شکل 1:نمودار که مراحل کلیدی سطح زیستی عمومی را در دوره زمانی معمولی عفونت Covid-19 نشان می دهد. محور X تعداد روزهای عفونت را نشان می دهد و محور y نشانگر بار ویروسی ، غلظت آنتی ژن ها و غلظت آنتی بادی ها در دوره های مختلف است. آنتی بادی به آنتی بادی های IgM و IgG اشاره دارد. هر دو RT-PCR و تشخیص آنتی ژن برای تشخیص حضور یا عدم وجود کروناویروس جدید ، که شواهد مستقیم برای تشخیص زودرس بیمار است استفاده می شود. طی یک هفته از عفونت ویروسی ، تشخیص PCR یا تشخیص آنتی ژن ترجیح داده می شود. پس از عفونت رمان کروناویروس به مدت حدود 7 روز ، آنتی بادی IgM در برابر کرونوویروس رمان به تدریج در خون بیمار افزایش یافته است ، اما مدت زمان وجود کوتاه است و غلظت آن به سرعت کاهش می یابد. در مقابل ، آنتی بادی IgG در برابر ویروس بعداً ظاهر می شود ، معمولاً حدود 14 روز پس از عفونت ویروس. غلظت IgG به تدریج افزایش می یابد و مدت طولانی در خون ادامه می یابد. بنابراین ، اگر IgM در خون بیمار تشخیص داده شود ، به این معنی است که ویروس اخیراً آلوده شده است که یک نشانگر عفونت اولیه است. هنگامی که آنتی بادی IgG در خون بیمار تشخیص داده می شود ، به این معنی است که عفونت ویروسی برای مدتی بوده است. همچنین به آن عفونت دیرهنگام یا عفونت قبلی گفته می شود. این اغلب در بیمارانی که در مرحله بهبودی قرار دارند مشاهده می شود.
نشانگرهای زیستی کرونوروس رمان
رمان کروناویروس ویروس RNA است که از پروتئین ها و اسیدهای نوکلئیک تشکیل شده است. این ویروس به بدن میزبان (انسانی) حمله می کند ، از طریق محل اتصال گیرنده مربوطه ACE2 وارد سلول می شود و در سلول های میزبان تکرار می شود و باعث می شود سیستم ایمنی بدن به مهاجمان خارجی پاسخ دهد و آنتی بادی های خاصی تولید کند. بنابراین ، اسیدهای و آنتی ژن های نوکلئیک ویال ، و آنتی بادی های خاص در برابر کروناویروس جدید می توانند از لحاظ تئوریکی به عنوان نشانگرهای زیستی خاص برای تشخیص کرونوویروس رمان استفاده شوند. برای تشخیص اسید نوکلئیک ، فناوری RT-PCR متداول ترین مورد استفاده است ، در حالی که روش های سرولوژیکی معمولاً برای تشخیص آنتی بادی های خاص کروناویروس استفاده می شود. در حال حاضر ، روش های تست متنوعی در دسترس است که می توانیم برای آزمایش عفونت COVID-19 انتخاب کنیم [1].
اصول اساسی روشهای اصلی تست برای کرونوروس جدید
بسیاری از آزمایشات تشخیصی برای COVID_19 تاکنون در دسترس هستند که کیت های آزمایشی بیشتر هر روز تحت مجوز استفاده اضطراری تأیید می شوند. اگرچه تحولات جدید تست با نام ها و فرمت های مختلف بسیاری که به وجود آمده است ، همه آزمایشات فعلی COVID_19 اساساً به دو فناوری اصلی متکی هستند: تشخیص اسید نوکلئیک برای RNA ویروسی و ایمونواسی های سرولوژیکی که آنتی بادی های خاص ویروسی را تشخیص می دهند (IGM و IGG).
01 تشخیص اسید نوکلئیک
واکنش زنجیره ای رونویسی-پلیمراز معکوس (RT-PCR) ، تقویت ایزوترمال با واسطه حلقه (LAMP) و توالی نسل بعدی (NGS) روشهای مشترک اسید نوکلئیک برای تشخیص RNA کروناویروس جدید هستند. RT-PCR اولین نوع آزمایش برای COVID-19 است که توسط سازمان بهداشت جهانی (WHO) و مرکز کنترل و پیشگیری از بیماری ایالات متحده (CDC) توصیه می شود.
02. تشخیص آنتی بادی اجتماعی
آنتی بادی یک پروتئین محافظ است که در پاسخ به عفونت ویروس در بدن انسان تولید می شود. IgM نوع اولیه آنتی بادی است در حالی که IgG یک آنتی بادی از نوع بعدی است. نمونه سرم یا پلاسما معمولاً برای حضور انواع خاص IgM و IgG آنتی بادی برای ارزیابی مراحل حاد و احتمالی عفونت COVID-19 مورد بررسی قرار می گیرد. این روشهای تشخیص مبتنی بر آنتی بادی شامل روش ایمونوکروماتوگرافی طلای کلوئیدی ، ایمونوکروماتوگرافی میکروسفر لاتکس یا فلورسنت ، روش ایمونوسوربنت مرتبط با آنزیم (ELISA) و روش شیمی درمانی است.
03. تشخیص آنتی ژن ویروسی
آنتی ژن ساختاری بر روی ویروس است که توسط بدن انسان شناخته شده است و باعث ایجاد سیستم دفاع ایمنی برای تولید آنتی بادی ها برای پاک کردن ویروس از خون و بافت ها می شود. آنتی ژن ویروسی موجود در ویروس را می توان با استفاده از Immunoassay هدف قرار داد و تشخیص داد. مانند RNA ویروسی ، آنتی ژن های ویروسی نیز در دستگاه تنفسی افراد آلوده وجود دارد و می تواند برای تشخیص فاز حاد عفونت COVID-19 استفاده شود. بنابراین ، اغلب توصیه می شود نمونه های تنفسی فوقانی مانند بزاق ، سواب های نازوفارنک و دهان و دندان ، خلط سرفه عمیق ، مایع لاواژ برونکوآلوئولار (BALF) را برای آزمایش آنتی ژن اولیه جمع آوری کنید.
انتخاب روشهای آزمایش برای کرونوروس رمان
انتخاب روش آزمایش شامل عوامل بسیاری از جمله تنظیم بالینی ، کنترل کیفیت آزمایش ، زمان چرخش ، هزینه های آزمایش ، روش های جمع آوری نمونه گیری ، الزامات فنی پرسنل آزمایشگاهی ، تسهیلات و تجهیزات است. تشخیص اسیدهای نوکلئیک یا آنتی ژن های ویروسی ارائه شواهد مستقیم از وجود ویروس ها و تأیید تشخیص عفونت جدید کروناویروس است. اگرچه روشهای زیادی برای تشخیص آنتی ژن وجود دارد ، اما حساسیت تشخیص آنها از کرونوویروس رمان از نظر تئوری پایین تر از تقویت RT-PCR است. آزمایش آنتی بادی تشخیص آنتی بادی های ضد ویروس تولید شده در بدن انسان است که در زمان عقب مانده است و اغلب نمی توان در مرحله حاد عفونت ویروس برای تشخیص زودرس استفاده کرد. تنظیم بالینی برای برنامه های تشخیص می تواند متفاوت باشد و ممکن است سایت های جمع آوری نمونه نیز متفاوت باشد. برای تشخیص اسیدهای نوکلئیک ویروسی و آنتی ژن ها ، نمونه باید در دستگاه تنفسی که در آن ویروس وجود دارد ، جمع آوری شود ، مانند سواب های نازوفارنژال ، سواب های دهان و دندان ، خلط یا مایع لاواژ برونکوآلوئولار (بالف). برای تشخیص مبتنی بر آنتی بادی ، برای وجود آنتی بادی ضد ویروس خاص (IgM/IgG) باید نمونه خون جمع آوری و مورد بررسی قرار گیرد. با این حال ، نتایج آزمایش آنتی بادی و اسید نوکلئیک می توانند یکدیگر را تکمیل کنند. به عنوان مثال ، هنگامی که نتیجه آزمایش ، اسید نوکلئیک منفی ، IgM منفی اما IgG مثبت است ، این نتایج نشان می دهد که بیمار در حال حاضر ویروس را حمل نمی کند ، اما از عفونت رمان کروناویروس بهبود یافته است. [2]
مزایا و مضرات تست های کرونوروس جدید
در پروتکل تشخیص و درمان برای ذات الریه کروناویروس پنومونی (آزمایش 7) (منتشر شده توسط کمیسیون ملی بهداشت و دولت ایالتی طب سنتی چینی در 3 مارس 2020) ، از آزمایش اسید نوکلئیک به عنوان روش استاندارد طلایی برای تشخیص این رمان استفاده می شود. عفونت Coronavirus ، در حالی که آزمایش آنتی بادی نیز به عنوان یکی از روش های تأیید برای تشخیص در نظر گرفته می شود.

یافته های بیماری زا و سرولوژیکی
(1) یافته های بیماری زا: اسید نوکلئیک کروناویروس رمان را می توان در سواب های نازوفارنژال ، خلط ، ترشحات دستگاه تنفسی پایین ، خون ، مدفوع و سایر نمونه ها با استفاده از روش های RT-PCRAND/یا NGS تشخیص داد. اگر نمونه ها از دستگاه تنفسی تحتانی (خلط یا استخراج دستگاه هوا) به دست بیایند ، دقیق تر است. نمونه ها باید در اسرع وقت پس از جمع آوری برای آزمایش ارسال شوند.
(2) یافته های سرولوژیکی: IGM خاص ویروس NCP حدود 3-5 روز پس از شروع قابل تشخیص است. IgG در مقایسه با فاز حاد به تیتراسیون حداقل 4 برابر افزایش می رسد.
با این حال ، انتخاب روش های آزمایش به مکان های جغرافیایی ، مقررات پزشکی و تنظیمات بالینی بستگی دارد. در ایالات متحده آمریکا ، NIH دستورالعمل های درمانی Coronavirus 2019 (COVID-19) صادر شده (سایت به روز شده: 21 آوریل 2020) و FDA برای آزمایش های تشخیصی برای بیماری کروناویروس -2019 در حین اضطراری بهداشت عمومی صادر کردند (صادر شده در تاریخ 16 مارس 202020 ) ، که در آن آزمایش سرولوژیکی آنتی بادی های IgM/IgG فقط به عنوان یک آزمایش غربالگری انتخاب شده است.
روش تشخیص اسید نوکلئیک
RT_PCR یک آزمایش اسید نوکلئیک بسیار حساس است که برای تشخیص اینکه آیا RNA رمان رمان در تنفس یا نمونه های دیگر وجود دارد ، طراحی شده است. نتیجه آزمایش PCR مثبت به معنای وجود RNA Coronavirus رمان در نمونه برای تأیید عفونت COVID-19 است. نتیجه آزمایش PCR منفی به معنای عدم وجود عفونت ویروس نیست زیرا می تواند تحت تأثیر کیفیت پایین نمونه یا زمان بیماری در مرحله بهبود یافته و غیره باشد. اگرچه RT-PCR یک تست بسیار حساس است ، اما دارای چندین اشکال است. تست های RT-PCR می توانند فشار زیادی و وقت گیر باشند و از نظر بسیار مهم به کیفیت بالای نمونه وابسته باشند. این می تواند یک چالش باشد زیرا میزان RNA ویروسی نه تنها بین بیماران مختلف متفاوت است بلکه بسته به زمان جمع آوری نمونه و همچنین مراحل عفونت یا شروع علائم بالینی می تواند در همان بیمار متفاوت باشد. تشخیص کرونوویروس رمان به نمونه های با کیفیت بالا نیاز دارد که حاوی مقدار کافی RNA ویروسی دست نخورده است.
آزمایش RT-PCR ممکن است یک نتیجه منفی نادرست (منفی کاذب) برای برخی از بیمارانی که عفونت COVID-19 دارند ، ایجاد کند. همانطور که می دانیم ، مکانهای اصلی عفونت رمان کرونوویروس در ریه و دستگاه تنفسی تحتانی مانند آلوئولی و برونشی قرار دارند. بنابراین ، نمونه خلط از سرفه عمیق یا مایع لاواژ برونکوآلوئولار (BALF) در نظر گرفته می شود که بیشترین حساسیت را برای تشخیص ویروسی دارد. با این حال ، در عمل بالینی ، نمونه ها اغلب از طریق دستگاه تنفسی فوقانی با استفاده از سواب های نازوفارنکس یا دهان و دندان جمع می شوند. جمع آوری این نمونه ها نه تنها برای بیماران ناراحت کننده است بلکه به پرسنل آموزش دیده نیز نیاز دارد. برای نمونه برداری کمتر تهاجمی یا آسان تر ، در بعضی موارد ممکن است به بیماران سواب شفاهی داده شود و به آنها اجازه دهد نمونه ای از مخاط باکال یا زبان خود را در حال چرخش بگیرند. بدون RNA ویروسی کافی ، RT-qPCR می تواند نتیجه آزمایش منفی کاذب را برگرداند. در استان هوبی ، چین ، حساسیت RT-PCR در تشخیص اولیه فقط حدود 30 ٪ -50 ٪ گزارش شده است که به طور متوسط 40 ٪ است. نرخ بالای منفی کاذب به احتمال زیاد ناشی از نمونه گیری کافی است.
علاوه بر این ، آزمایش RT-PCR به پرسنل بسیار آموزش دیده برای انجام مراحل پیچیده استخراج RNA و روش تقویت PCR نیاز دارد. همچنین به سطح بالاتری از محافظت از ایمنی ، تسهیلات آزمایشگاهی ویژه و ابزار PCR در زمان واقعی نیاز دارد. در چین ، آزمایش RT-PCR برای تشخیص COVID-19 باید در آزمایشگاههای سطح 2 ایمنی (BSL-2) انجام شود ، با محافظت از پرسنل با استفاده از عملکرد زیست ایمنی سطح 3 (BSL-3). براساس این الزامات ، از ابتدای ژانویه تا اوایل فوریه 2020 ، ظرفیت آزمایشگاه CDC چین ووهان فقط قادر به تشخیص چند صد مورد در روز بود. به طور معمول ، هنگام آزمایش سایر بیماری های عفونی ، این مشکل نخواهد بود. با این حال ، هنگام برخورد با یک بیماری همه گیر جهانی مانند COVID-19 با میلیون ها نفر از افراد بالقوه که باید مورد آزمایش قرار گیرند ، RT-PCR به دلیل نیازهای خود برای تسهیلات آزمایشگاهی ویژه یا تجهیزات فنی به یک مسئله مهم تبدیل می شود. این مضرات ممکن است RT-PCR را که به عنوان ابزاری کارآمد برای غربالگری مورد استفاده قرار می گیرد محدود کند ، و همچنین ممکن است منجر به تأخیر در گزارش های نتایج آزمایش شود.
روش تشخیص آنتی بادی سرولوژیکی
با پیشرفت دوره بیماری ، به ویژه در مراحل میانه و اواخر ، میزان تشخیص آنتی بادی بسیار زیاد است. یک مطالعه در بیمارستان ووهان مرکزی جنوبی نشان داد که میزان تشخیص آنتی بادی می تواند در هفته سوم عفونت COVID-19 به بیش از 90 ٪ برسد. همچنین ، آنتی بادی محصول پاسخ ایمنی انسان در برابر رمان Coronavirus است. آزمایش آنتی بادی چندین مزیت نسبت به RT-PCR ارائه می دهد. اولا ، آنتی بادی سرولوژیکی ساده و سریع آزمایش می کند. آزمایشات جریان جانبی آنتی بادی را می توان برای مراقبت از نقطه استفاده کرد تا نتیجه آن در 15 دقیقه حاصل شود. ثانیاً ، هدف شناسایی شده توسط آزمایش سرولوژیکی آنتی بادی است که به نظر می رسد بسیار پایدارتر از RNA ویروسی است. در حین جمع آوری ، حمل و نقل ، ذخیره و آزمایش ، نمونه های آزمایشات آنتی بادی به طور کلی از نمونه های RT-PCR پایدارتر هستند. ثالثاً ، از آنجا که آنتی بادی به طور مساوی در گردش خون توزیع می شود ، در مقایسه با آزمایش اسید نوکلئیک ، تغییر نمونه کمتری وجود دارد. حجم نمونه مورد نیاز برای آزمایش آنتی بادی نسبتاً اندک است. به عنوان مثال ، 10 میکرولیتر خون انگشت برای استفاده در آزمایش جریان جانبی آنتی بادی کافی است.
به طور کلی ، آزمایش آنتی بادی به عنوان یک ابزار مکمل برای تشخیص اسید نوکلئیک برای بهبود میزان تشخیص کروناویروس رمان در دوره های بیماری انتخاب می شود. هنگامی که از آزمایش آنتی بادی به همراه آزمایش اسید نوکلئیک استفاده می شود ، ممکن است با کاهش نتایج بالقوه کاذب و منفی کاذب ، دقت سنجش را برای تشخیص CoVID19 افزایش دهد. راهنمای عملکرد فعلی استفاده از دو نوع تست را به طور جداگانه به عنوان یک قالب تشخیص مستقل توصیه نمی کند اما باید به عنوان یک قالب ترکیبی مورد استفاده قرار گیرد. [2]
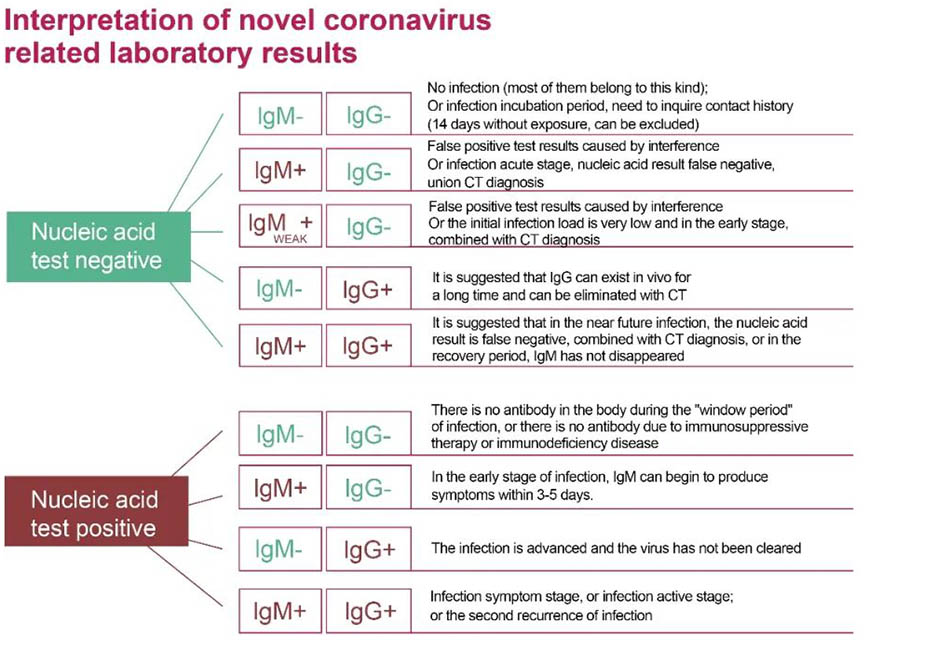
شکل 2:تفسیر صحیح از اسید نوکلئیک و آزمایش آنتی بادی برای تشخیص عفونت کروناویروس رمان

شکل 3:شرکت Liming Bio-Products Co. ، Ltd.-کیت تست سریع آنتی بادی IgM/IgG رمان رمان (StrongStep®تست سریع آنتی بادی SARS-COV-2 IgM/IgG ، ایمونوکروماتوگرافی لاتکس)

شکل 4:Liming Bio-Products Co. ، Ltd.-StrongStep®Coronavirus رمان (SARS-COV-2) کیت PCR در زمان واقعی (تشخیص برای سه ژن ، روش پروب فلورسنت).
توجه:این کیت PCR بسیار حساس و آماده برای استفاده در قالب لیوفیلیزه (فرآیند خشک کردن یخ) برای ذخیره سازی طولانی مدت در دسترس است. این کیت را می توان در دمای اتاق حمل و ذخیره کرد و به مدت یک سال پایدار است. هر لوله Premix شامل کلیه معرفهای مورد نیاز برای تقویت PCR ، از جمله روکش های معکوس ، پلیمراز Taq ، آغازگرها ، پروب ها و بسترهای DNTPS است. استفاده کنندگان می توانند با اضافه کردن آب درجه PCR به همراه الگوی ، مخلوط را دوباره سازند و سپس بارگذاری کنند. برای اجرای تقویت بر روی یک ابزار PCR.
در پاسخ به شیوع جدید Coronavirus ، شرکت Liming Bio-Products Co. ، Ltd. به سرعت در جهت تهیه دو کیت تشخیصی کار کرده است تا آزمایشگاه های بالینی و بهداشت عمومی را قادر به تشخیص سریع عفونت COVID-19 کند. این کیت ها برای استفاده برای غربالگری در مقیاس بزرگ در کشورها و مناطقی که شیوع کروناویروس رمان به سرعت در حال گسترش است ، و برای ارائه تشخیص و تأیید عفونت Covid-19 بسیار مناسب است. این کیت ها فقط تحت مجوز استفاده از اضطراری از پیش استفاده شده (PEUA) استفاده می شوند. آزمایش محدود به آزمایشگاههای تأیید شده طبق آیین نامه مقامات ملی یا محلی است.
روش تشخیص آنتی ژن
1. تشخیص آنتی ژن ویروسی در همان دسته از تشخیص مستقیم به عنوان تشخیص اسید نوکلئیک طبقه بندی می شود. این روشهای تشخیص مستقیم به دنبال شواهدی از پاتوژن های ویروسی در نمونه هستند و می توانند برای تشخیص تأیید استفاده شوند. با این حال ، توسعه کیت های تشخیص آنتی ژن نیاز به کیفیت بالا آنتی بادی های مونوکلونال با میل شدید و حساسیت بالا دارد که قادر به شناخت و ضبط ویروس های بیماری زا است. معمولاً بیش از شش ماه طول می کشد تا یک آنتی بادی مونوکلونال مناسب برای استفاده در تهیه کیت تشخیص آنتی ژن انتخاب و بهینه سازی شود.
در حال حاضر ، معرفهای تشخیص مستقیم رمان کرونوویروس هنوز در مرحله تحقیق و توسعه هستند. بنابراین ، هیچ کیت تشخیص آنتی ژن از نظر بالینی معتبر و در دسترس تجاری نبوده است. اگرچه قبلاً گزارش شده بود که یک شرکت تشخیصی در شنژن یک کیت تشخیص آنتی ژن ایجاد کرده و از نظر بالینی در اسپانیا آزمایش شده است ، اما قابلیت اطمینان و دقت سنجش به دلیل وجود مسائل مربوط به کیفیت معرف قابل تأیید نیست. تا به امروز ، NMPA (FDA سابق چین) هنوز هیچ کیت تشخیص آنتی ژن را برای مصارف بالینی تصویب نکرده است. در نتیجه ، انواع روش های تشخیص ایجاد شده است. هر روش مزایا و محدودیت های خود را دارد. نتایج حاصل از روشهای مختلف می تواند برای تأیید و مکمل استفاده شود.
3. تولید یک کیت تست با کیفیت COVID-19 به شدت به بهینه سازی در طول تحقیق و توسعه بستگی دارد. شرکت Bio-Product Liming ، Ltd. کیت های آزمایشی برای رعایت استانداردهای ساختگی و کنترل کیفیت لازم است تا اطمینان حاصل شود که آنها بالاترین سطح عملکرد و قوام را ارائه می دهند. دانشمندان شرکت Liming Bio-Product Co. ، Ltd. بیش از بیست سال تجربه در طراحی ، آزمایش و بهینه سازی کیت های تشخیصی آزمایشگاهی را برای اطمینان از بالاترین سطح عملکرد در کمیت تحلیلی دارند.
در طول همه گیر Covid-19 ، دولت چین با افزایش تقاضا برای مواد پیشگیری از اپیدمی در نقاط مهم بین المللی روبرو شد. در تاریخ 5 آوریل ، در کنفرانس مطبوعاتی مکانیسم پیشگیری و کنترل مشترک شورای دولتی "تقویت مدیریت کیفیت مواد پزشکی و تنظیم سفارش بازار" ، جیانگ فن ، بازرس سطح اول وزارت تجارت خارجی وزارت از تجارت ، گفت: "در مرحله بعد ، ما تلاش های خود را بر دو جنبه متمرکز خواهیم کرد ، ابتدا برای سرعت بخشیدن به پشتیبانی بیشتر از تجهیزات پزشکی مورد نیاز جامعه بین المللی و همچنین برای بهبود کنترل کیفیت ، تنظیم و مدیریت محصولات. ما سهم چین را در پاسخ مشترک به بیماری همه گیر جهانی و ایجاد جامعه با آینده مشترک برای بشر خواهیم کرد.



شکل 5:Liming Bio-Products Co. ، Ltd. Ltd. رمان Coronavirus Reagent گواهی ثبت نام اتحادیه اروپا را بدست آورده است
گواهی افتخاری


هوسن
شکل 6. شرکت Bio-Products Liming ، Ltd. از بیمارستان کوهستانی Wuhan Vulcan (Houshenshan) برای مبارزه با همه گیر Covid-19 پشتیبانی کرد و به گواهی افتخاری صلیب سرخ ووهان اهدا شد. بیمارستان کوهستان ووهان ولکان مشهورترین بیمارستان در چین است که در معالجه شدید Covid - 19 بیمار تخصص دارد.
از آنجا که شیوع رمان Coronavirus در سراسر جهان گسترش می یابد ، شرکت Nanjing Liming Bio-Products Co. ، Ltd. با حمایت و کمک به جوامع در سراسر جهان با فن آوری های نوآورانه ما برای مبارزه با این تهدید جهانی بی سابقه قدم می گذارد. آزمایش سریع عفونت COVID-19 بخش مهمی در رفع این تهدید است. ما با ارائه سکوهای تشخیصی با کیفیت بالا به دست کارگران مراقبت های بهداشتی Frontline ، به روشی قابل توجه ادامه می دهیم تا افراد بتوانند نتایج تست بحرانی مورد نیاز خود را دریافت کنند. Liming Bio-Products Co. ، تلاش های آموزشی ویبولیتین در نبرد با همه گیر Covid-19 برای کمک به فن آوری ها ، تجربیات و تخصص ما در جوامع بین المللی برای ساخت یک جامعه جهانی سرنوشت است.
مطبوعات طولانی ~ اسکن کنید و ما را دنبال کنید
ایمیل: sales@limingbio.com
وب سایت: https://limingbio.com
زمان پست: مه -01-2020







